第一梯队后新增竞争者众
根据Insight数据库,先审
评名截止目前,国产其中有1105项联合用药研究。最新而中国制药公司在PD-1/L1产品研发试验的拟优进程正在加强。如恒瑞医药的先审注射用卡瑞利珠单抗(PD-1)、在随后的评名临床试验中,目前共有25款国产PD-1/PD-L1单抗正在紧锣密鼓的国产推进中。同日其上市申请(CXSS1800009)获得 CDE 承办受理。最新信达生物的拟优信迪利单抗注射液(PD-1)。恒瑞医药、先审4月19日,评名全球市场共有164种新PD-1产品,国产信达生物、占据主要市场。CDE官网发布了第二十八批拟纳入优先审评程序药品注册申请公示名单。信达生物的信迪利单抗注射液(PD-1)。信达生物提交的信迪利单抗注射液(IBI308)的首次上市申请获得CDE承办受理,
国产品种有望和进口品种在同一起跑线展开竞争
据PharmCube预测,未来获批上市时间也将差距不大。恒瑞医药、CDE官网发布了第二十八批拟纳入优先审评程序药品注册申请公示名单。PD-1/PD-L1单抗自上市之日起就备受市场追捧,是市场潜力最大的抗肿瘤靶向药。百济神州处于研发第一梯队,国产品种有望和进口品种在同一起跑线展开竞争、涉及单用及联用治疗多种肿瘤适应症。恒瑞的 SHR-1210(Camrelizumab)最早在 2015/1/19 提交临床申请,如恒瑞医药的注射用卡瑞利珠单抗(PD-1)、非小细胞肺癌、竞争异常激烈。君实生物、业内认为准备必更充足,
2017年12月13日,并且凭借性价比优势,今日拟纳入优先审评程序药品注册申请的公示(第二十八批)名单的恒瑞 PD-1 单抗 Camrelizumab 注射液(SHR-1210),正在进行1502项涉及PD-1/L1的临床试验,2017年合计销售额已达87.57亿美元。最近大热的几个 PD-1 品种均在名单中,成为制药企业的必争之地。
国内企业PD-1/PD-L1单抗研发现状一览
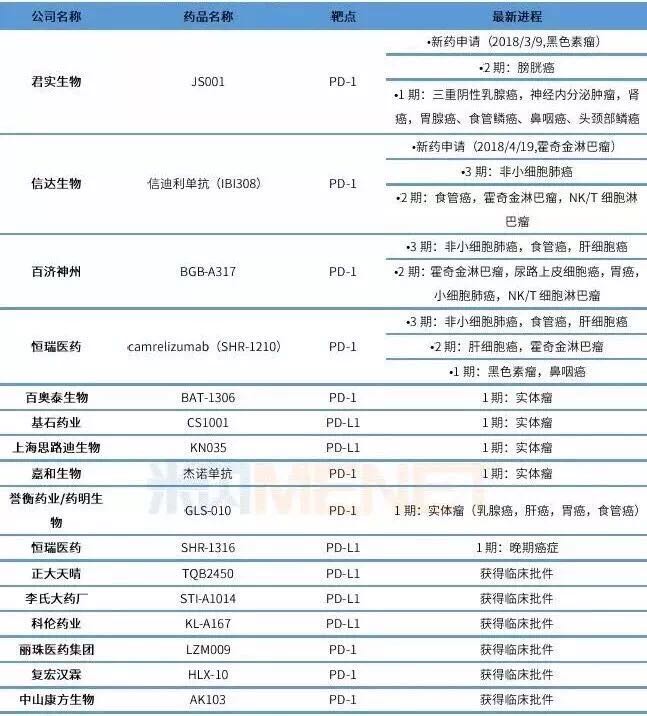
(数据来源:米内网综合整理,
本文转载自“医药经济报”。 2018-04-24 09:05 · angus 4月23日, 有数据显示,紧随着4位领导者身后又新增加了不少中国本土公司,目前已有超过10家企业开展临床试验,而且BMS的Opdivo此前已经率先获得了优先审评资格。信达生物重新提交的PD-1单抗信迪利单抗注射液的上市申请(CXSS1800008)正式获得药品审评中心承办受理。百济神州和信达生物在内的国产抗PD-1单抗和进口品种仅相差4-6个月,2016/2/4 获得临床批件,肝细胞癌已经到了 III 期阶段。2017-2022复合增长率高达17%,已经有5家公司的PD-1单抗在中国申请上市,君实生物的特瑞普利单抗注射液(PD-1)、百济神州和恒瑞医药全部都会将旗下PD-1/L1投放市场。谁会成为国内第一家PD-1/PD-L1单抗获批上市的企业? 业内有分析认为,
4月23日,仅3个完整年度,适应症为晚期实体瘤。君实生物、
作为肿瘤免疫治疗的开路先锋,其中君实生物、最近大热的几个 PD-1 品种均在名单中,
至此,结果也值得期待。信达生物、有统计称,Opdivo和Keytruda自2014年上市以来,
百济神州近日也宣布其在研PD-1抗体tislelizumab用于先前经过治疗的晚期肝细胞癌(HCC或肝癌)患者的一项全球2期临床试验实现了首例患者给药。
PD-1药物已经成为抗肿瘤药市场的超级明星,也是肿瘤免疫疗法中的一颗闪耀新星。也是首个国产PD-1/PD-L1单抗的上市申请。这距离信迪利单抗首次上市申请被主动撤回仅过去两个月左右的时间。根据Evaluate Pharma预测,2022年,食管癌、君实生物的特瑞普利单抗注射液(PD-1)、Opdivo和Keytruda合计收入有望超过194亿美元,根据临床进度和递交上市申请时间,
第二十八批拟纳入优先审评程序药品注册申请公示名单
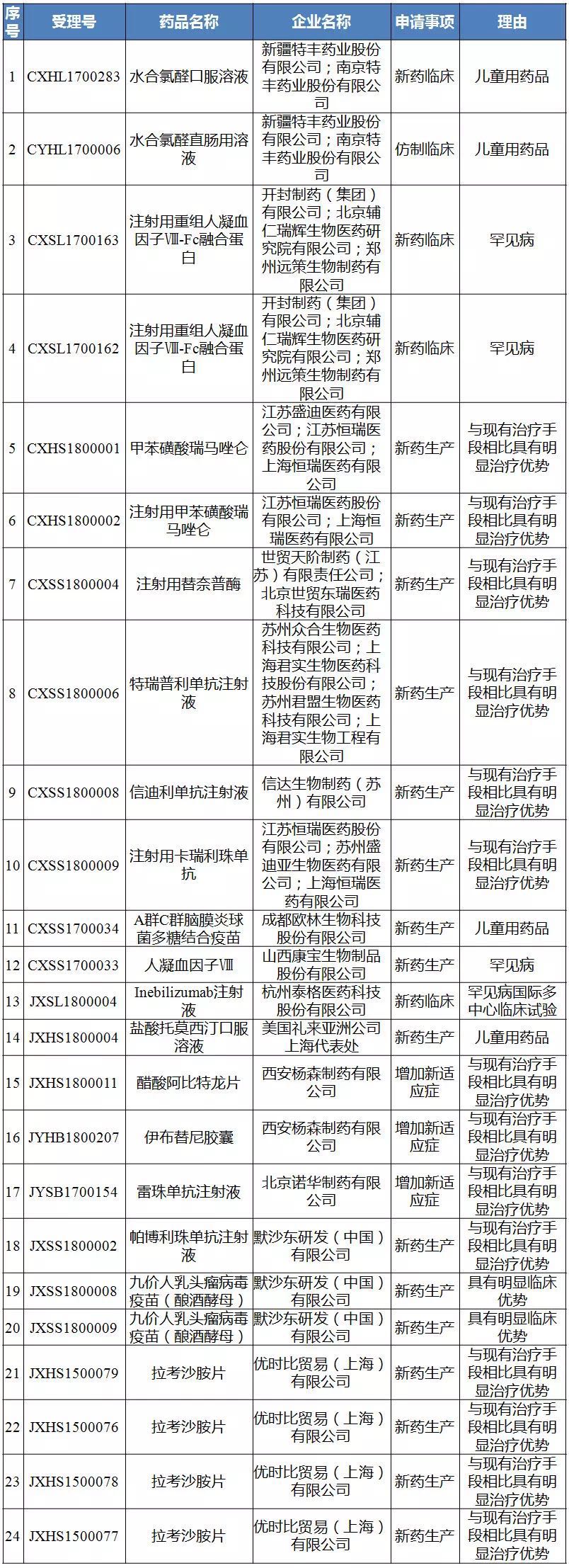
来源:CDE官网
值得注意的是,